论文题目:Single-cell identification, drug susceptibility test and whole-genome sequencing of Helicobacter pylori directly from gastric biopsy by Clinical Antimicrobial Susceptibility Test Ramanometry
发表期刊:Clinical Chemistry《临床化学》杂志(影响因子:8.327)
发表时间:2022年6月18日
作者单位:中国科学院青岛生物能源与过程研究所、青岛星赛生物科技有限公司、中国疾病预防控制中心传染病预防控制所、青岛市立医院等
引言
我国幽门螺杆菌(H. pylori)感染呈现高感染率(约50%)、高疾病负担、高耐药率和低根除率特征,而低根除率的主要原因之一为幽门螺杆菌菌株耐药严重。因此,建立一个高效的药敏诊断、治疗与溯源体系,对于临床和相关疾病防控至关重要。青岛能源所与中国疾控中心传染病所、青岛市立医院等团队联合,依托星赛生物的临床单细胞拉曼药敏快检仪(CAST-R),利用重水标记单细胞拉曼光谱技术(D₂O-SCRS),建立了单个细菌细胞精度、“鉴定-药敏-溯源”全流程一体化的H. pylori诊疗技术CAST-R-HP,具有快速病原鉴定、精确药敏表型检测、基于单细胞全基因组支撑耐药机制研究与精准溯源等优势。
成果介绍
本研究构建了15种临床常见胃部共生菌的单细胞拉曼光谱(SCRS)参考数据库,利用端到端的深度卷积神经网络(DCNN),融合了拉曼光谱特征提取与分类模型训练过程,将SCRS的病原鉴定准确率提升至98.5±0.27%。并且,研究人员建立了单细胞精度测定代谢抑制程度的H. pylori药敏表型快检技术。与临床标准E-test法相比,17株H. pylori临床分离株对左氧氟沙星、克拉霉素的药敏检测准确率分别为94%和100%。此外,还直接测定了7例患者胃粘膜组织样本中H. pylori对于左氧氟沙星的药敏性,准确率达100%。最后,研究人员利用拉曼光镊液滴单细胞分选(RAGE)芯片,完成了高均衡性的目标单细胞分选和核酸扩增,单细胞全基因组覆盖度可达99.7%,通过基因型验证了药敏表型。
图文导读
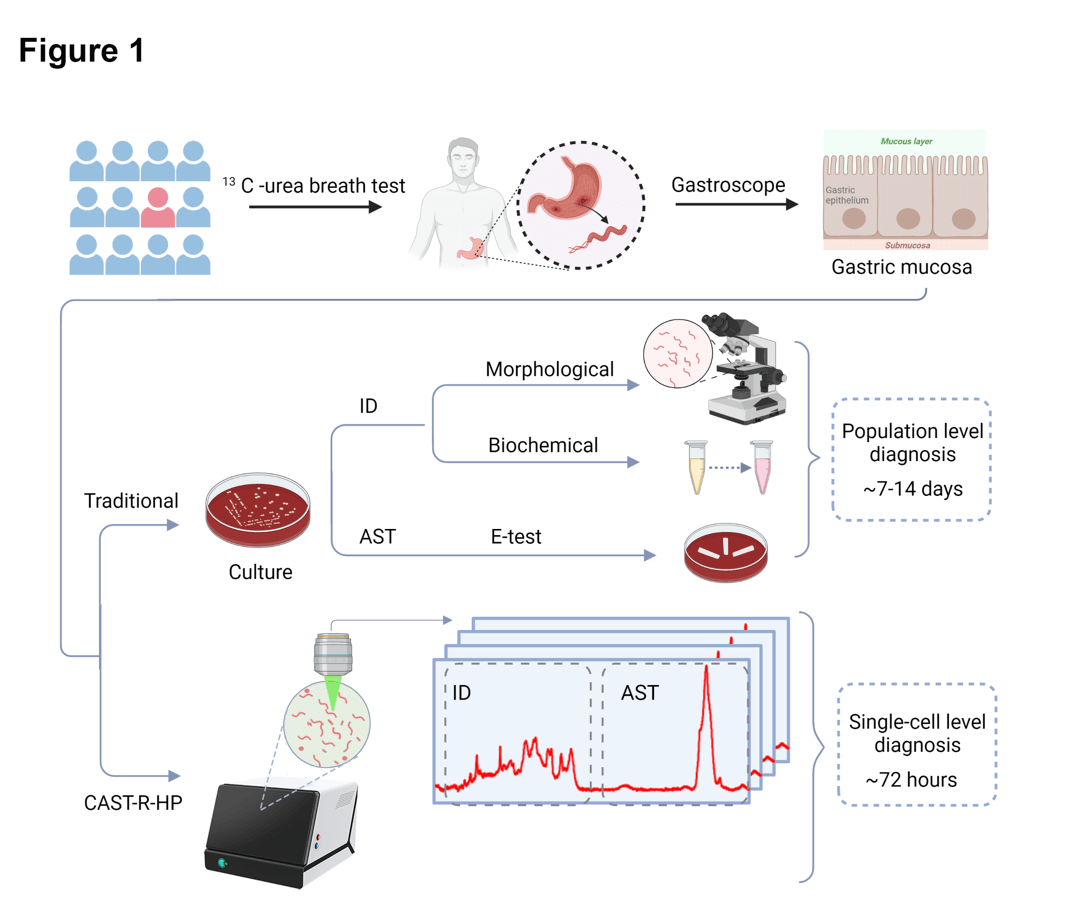
图1. CAST-R-HP工作流程。从临床胃活检样本出发进行菌株鉴定(ID)和药敏检测(AST),传统方法需要7-14天,CAST-R-HP方法需要72小时。
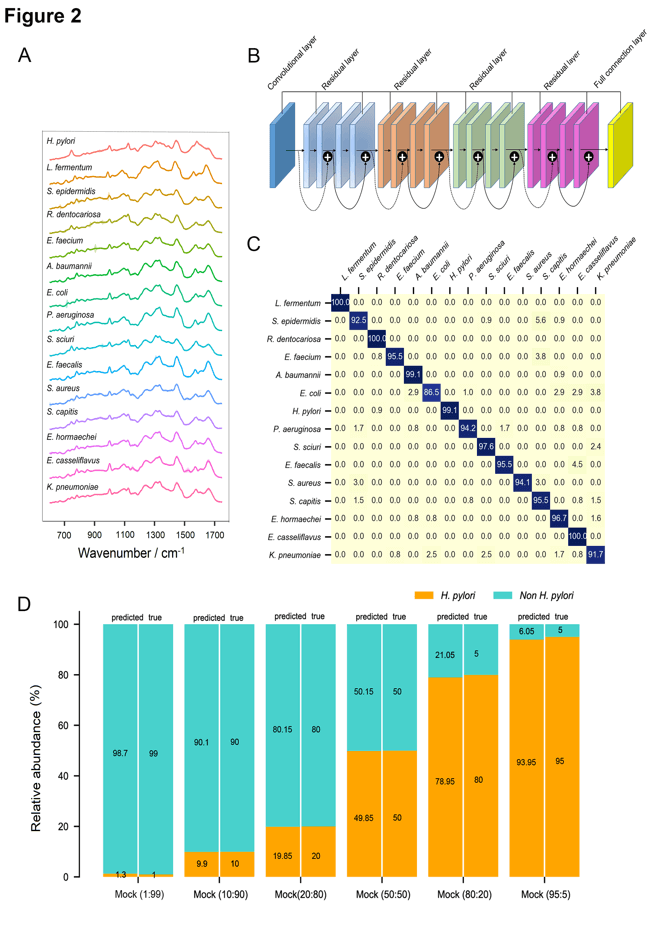
图2. 基于单细胞拉曼光谱(SCRS)直接从临床胃活检样本中鉴定H. pylori。(A)不同临床菌株的拉曼光谱区分度较小。15个分离株各自600条光谱的平均光谱以粗体显示,代表了每个分离株的特征;(B)利用18层的1维残差神经网络对15个类别的拉曼光谱进行分类;(C)15个类别预测结果的混淆矩阵。对角线上的数值表示每个类别的预测准确率;(D)人工模拟样本的预测相对丰度和真实相对丰度的对比(人工模拟样本中H. pylori光谱和其他14种菌光谱由不同比例组成)。
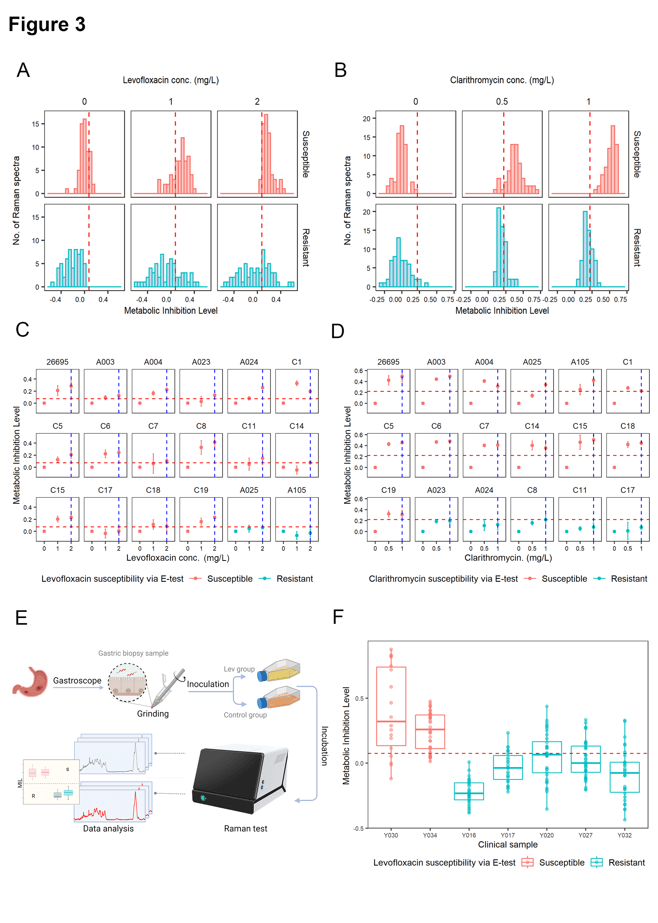
图3. 基于CAST-R-HP的H. pylori药敏表型快检技术,包括纯培养和临床胃活检样本。(A) 0、1、2 mg/L左氧氟沙星对H. pylori代谢水平抑制程度,菌种选用左氧氟沙星敏感株(H. pylori ATCC 26695)和左氧氟沙星耐药株 (H. pylori A105);(B)0、0.5、1 mg/L克拉霉素对H. pylori代谢水平抑制程度,菌种选择克拉霉素敏感株(H. pylori ATCC 26695)和克拉霉素耐药株(H. pylori A024);代谢水平抑制程度阈值验证(C)和(D)。红线为测定药敏的标准;(E)临床胃活检样本的药敏检测(AST)流程;(F)7例胃活检样本MIL截断值的验证(2 mg/L左氧氟沙星孵育3天)。
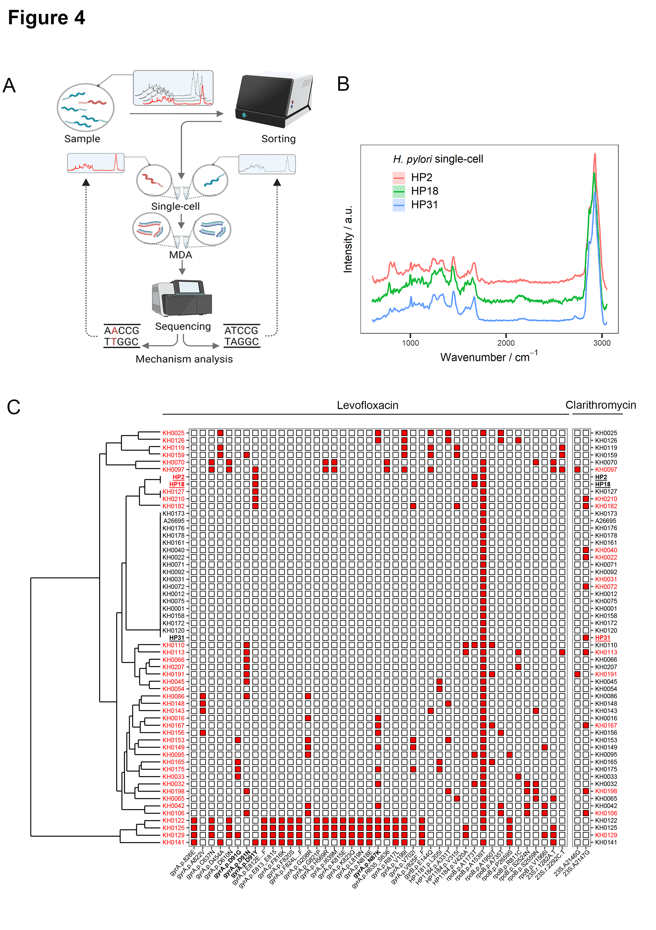
图4. 利用拉曼光镊液滴单细胞分选技术完成临床样本中单个H. pylori抗性突变体的筛选,并对其进行全基因组测序。(A)对临床胃活检样本中H. pylori进行单细胞拉曼分选和测序(RAGE-Seq)的工作流程;(B)Y027样品的HP2和HP18细胞在左氧氟沙星作用下SCRS中出现C-D峰,表示代谢活性强(即对左氧氟沙星具有抗性,而Y030样品的HP31细胞则对左氧氟沙星敏感);(C)基于57个H. pylori全基因组测序数据、耐左氧氟沙星(Lev)/克拉霉素(Clr)相关基因、药敏表型,用最大似然法构建系统发育树(包括通过RAGE-Seq获得的直接来源于临床样本的单细胞基因组HP2,HP18和HP31,54个来自纯培养分离株的全基因组)。耐药表型用红色表示。
总结
本研究建立的“鉴定-药敏-溯源”全流程一体化的H. pylori 诊疗技术CAST-R-HP,能够兼备在单细胞分辨率下快速识别、基于表型的AST和基于基因组的耐药机制研究的特点,该方法从临床样品到药敏结果的完整流程可大幅缩短至3天。未来,通过在单细胞分辨率下建立的代谢表型与相应耐药基因型之间的联系,有助于在单个患者或易感人群中绘制H. pylori耐药谱图,从而实现对患者的精准用药,降低耐药性的传播。CAST-R是星赛生物推出的针对临床应用市场的药敏快检仪器,基于创新的重水标记单细胞拉曼药敏快检技术(D₂O-Ramanometry),CAST-R通过与北京协和医院、青岛市立医院、青岛大学附属医院、浙江大学医学院附属邵逸夫医院等临床团队的密切合作,开发和示范了针对血液、口腔护理、胃粘膜等样品类型或场景的临床药敏快检流程,并进行了较为系统与深入的临床样品测试。基于“微生物药敏单细胞技术临床示范网络(SinCheckNet)”,星赛生物将进一步开发CAST-R-HP系统,拓展其应用,从而为建立单细胞精度的诊疗与疾控体系奠定技术和装备基础。














 鲁公网安备37021202001515
鲁公网安备37021202001515


